Laboratorní technika/Infračervená spektroskopie
Základní údaje
[editovat | editovat zdroj]Infračervená spektroskopie pracuje se zářením v infračervené oblasti elektromagnetického spektra, která se nachází v intervalu 0,78 až 1000 μm. Tuto oblast můžeme rozdělit na tři části:
- Blízká infračervená oblast (0,78 - 2,5 μm, tj. 12800 - 4000 cm-1)
- Střední infračervená oblast (2,5 - 50 μm, tj. 4000 - 200 cm-1)
- Vzdálená infračervená oblast (50 - 1000 μm, tj. 200 - 10 cm-1)
Je to soubor metod, které využívají vlastností molekul spojených s přítomností kovalentních a koordinačních vazeb. Kovalentní vazba mezi dvěma stejnými atomy je zprostředkována jednoho sdílením elektronového páru (v molekule Cl2), respektive dvou (O2) či tří (N2) elektronových párů. I mezi různými atomy může probíhat sdílení elektronových párů stejně jako jeden atom může sdílet své elektrony s více různými atomy (H2O, NH3). Koordinačně kovalentní vazba vznikne, když jeden z atomů doplní do vazby oba elektrony z jednoho elektronového páru.
Infračervené záření má nižší frekvenci a delší vlnovou délku než viditelné světlo. Infračervená spektroskopie patří mezi absorpční techniky, to znamená, že spektrum vzniká absorpcí záření daným vzorkem. Během absorpce dochází k excitaci molekuly na vyšší vibrační a rotační hladiny. V oblasti IR se místo frekvence udává vlnočet a vlnová délka se udává v mikrometrech. U tohoto způsobu spektroskopie se využívá faktu, že se různé molekuly po absorpci IR záření určité frekvence chovají jinak vzhledem ke svému složení. Tyto odlišnosti jsou způsobeny různou energií molekul, délkami vazeb a vnitřním pohybem atomů v molekulách. Zde je ukázka vibračních pohybů v molekule:
| Symmetrické | Antisymmetrické |
|---|---|
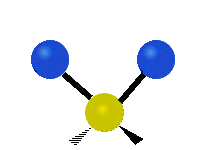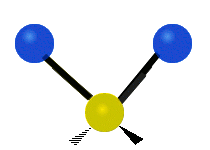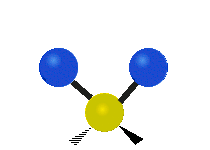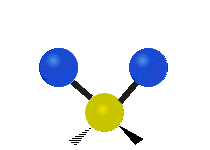 Symetrická valenční vibrace |
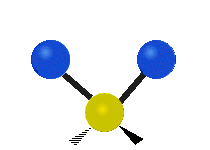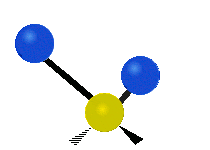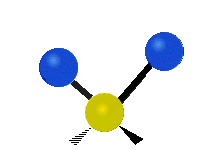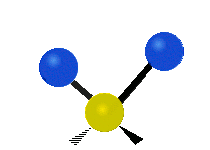 Antisymetrická valenční vibrace |
 Nůžková vibrace |
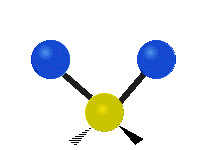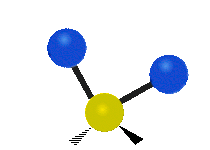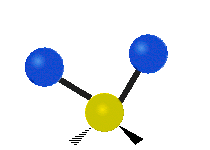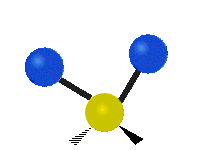 Rocking |
 Wagging |
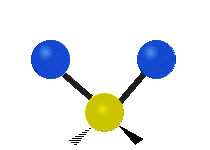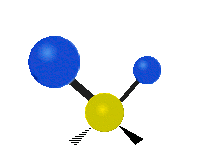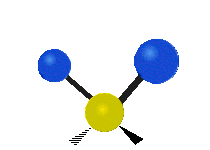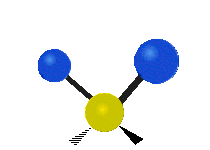 Twisting |
Když molekula absorbuje foton o vlnové délce spadající do infračerveného spektra, změní se její vibrační pohyb, což lze zaznamenat právě díky infračervené spektroskopii. Množství energie molekuly není možné měnit libovolně, ale energie je kvantována, což znamená, že molekula může vibrovat jen v určitých frekvencích, které odpovídají daným hladinám energie.

Například délky vazeb nejsou vždycky pevně dané hodnoty, ale jde o průměr hodnot délky, kterých vazba dosahuje. Vazba C-H o průměrné délce 110 pm ve skutečnosti kmitá s určitou frekvencí, střídavě se zkracuje a natahuje do hodnot, jejichž průměr je 110 pm. Pokud molekulu ozáříme elektromagnetickým zářením, pohltí energii, pokud energie záření odpovídá rozdílu energií vibračních nebo rotačních hladin. Výsledkem absorpce energie je, že se zvýší amplituda vibrace neboli vazba se zkracuje a natahuje o něco více. Protože určitá frekvence záření pohlceného molekulou odpovídá určitému molekulovému pohybu, můžeme poznat typy molekulových vibrací látky tím, že změříme její infračervené spektrum. Jeho následnou interpretací můžeme zjistit, jaké druhy vazeb či funkčních skupin jsou přítomny v molekule dané látky.
Průběh měření
[editovat | editovat zdroj]IR spektra můžeme měřit v transmisním nebo reflexním módu. V transmisním módu necháme záření procházet vzorkem a měříme závislost množství absorbovaného záření na energii. Protože vzorky bez úpravy by absorbovaly veškeré záření ze zdroje, je nutné je naředit látkou s nízkým molárním absorpčním koeficientem. Vzorky pro IR spektroskopii se běžně měří ve formě tablet z bromidu draselného nebo suspenze v minerálním oleji Nujol. Lze měřit i kapalné a plynné látky. Kapaliny měříme jako tenký film mezi stěnami z vhodného materiálu, nejčastěji \ce{KBr}, a plyny měříme v plynových kyvetách, které jsou konstruované tak, aby dráha paprsku byla co nejdelší, protože v plynném skupenství jsou od sebe molekuly dané látky vzdáleny více než v pevném či kapalném.
KBr tablety se připravují smísením a homogenizací suchého bromidu draselného se vzorkem (1-3 hm.%). Připravená směs se poté lisuje v hydraulickém lisu působením tlaku přibližně 10 tun po dobu 1 minuty. Během měření prochází paprsek záření připravenou tabletou a dopadá na detektor, který zaznamenává prošlé záření.
V reflexi se nejčastěji měří s využitím metody ATR (Attenuated Total Reflection - zeslabený úplný odraz). Vzorek se nanese na krystal z vhodného materiálu (diamant, ZnSe, Ge, Si), přitlačí se ocelovým hrotem a měří se. Výhodou této metody je možnost měření vzorku bez úprav, nevýhodou je měření pouze povrchové vrstvy vzorku, infračervené záření pronikne pouze do hloubky 1-3 μm. Paprsek prochází krystalem pod mezním úhlem, kdy nedochází k lomu, ale pouze k odrazu. Při dopadu na rozhraní krystal/vzorek dochází ke vzniku spektra. Spektrometr je jednopaprskový, je tedy nezbytné naměřit pozadí a až poté spektra vzorku. Aby vznikl finální graf, je nutné od spektra vzorku odečíst spektrum pozadí.
Zdroj vyšle záření v daném spektru, část záření je absorbováno vzorkem s danou molekulou a na detektoru se zachytí zbylé světlo, které prošlo skrz. Výsledný graf zobrazuje buď absorpční nebo transmisní spektrum.
Absorbance a transmitance
[editovat | editovat zdroj]Množství absorbovaného záření lze zaznamenat dvěma způsoby. Absorbance popisuje jaká část záření při dané energii se absorbovala vzorkem. Pro přepočet transmitance na absorbanci použijeme vzorec A = -log(T) Kde A je absorbance a T je transmitance.
Transmitance určuje, kolik záření projde vzorkem na detektor.
Lambertův-Beerův zákon se využívá při kvantitativním stanovení složení směsí. Tento zákon popisuje přímou úměru mezi absorbancí a koncentrací absorbující látky a vyjadřuje množství absorbovaného světla:
A = ε * l * c
Kde ε je molární absorpční koeficient (schopnost látky absorbovat světlo), l délka kyvety a c je molární koncentrace
Pro kvantitativní stanovení se snažíme vybírat pásy, jejichž hodnota molárního absorpčního koeficientu je co nejvyšší a u kterých je splněna lineární závislost absorbance na koncentraci.
Využití
[editovat | editovat zdroj]Výhodou IR spektroskopie je nízká spotřeba vzorku, případně nedestruktivnost metody, při použití bezkontaktního spektrometru či infračerveného mikroskopu. Tohoto faktu lze využít například u restaurování a konzervování uměleckých děl. Této metody lze využít při analýze povrchových vrstev, pigmentů, barviv.
Obvykle se využívá v chemii při analýze produktů a výchozích látek, dále se využívá v průmyslu pro kontrolu čistoty vstupních látek, meziproduktů i produktů.
V lékařství lze tuto metodu využít ke studiu biologických systémů, tedy lipidů, proteinů, nukleových kyselin a pod.
Mezi speciální aplikace patří například datování dřeva, které může být pro mladší dřevěné předměty podstatně přesnější než datování pomocí měření rozpadu radionuklidu \ce{^{14}C}.
Jednou z dalších výhod je cena přístrojů na tuto metodu. Zařízení určené k jedné metodě měření, tj. bez výměnné jednotky, například ATR, lze koupit v ceně okolo půl milionu korun českých i s krystalem z přírodního diamantu, což je značně méně než přístroje s výměnnou jednotkou (které jsou značně univerzálnější), jejichž cena se pohybuje od 4 milionů výše.
Spektrometr
[editovat | editovat zdroj]
Na obrázku vidíme spektrometr Bruker Tensor 27, který se skládá z několika částí viditelně oddělených. Vlevo vpředu je pyroelektrický detektor. Uprostřed je výměnná jednotka Platinum ATR, na kterou se umisťuje vzorek a na které se měří v reflexi pomocí diamantu. Paprsek záření vstoupí do krystalu pod tzv. mezním úhlem, kdy se paprsek neláme, ale pouze odráží. Během odražení se paprsek dostane ke vzorku na délku jedné vlny, poté projde diamantem a dopadne na detektor. Vpravo je soustava zrcadel, která se nazývá Michelsonův interferometr.

Beamsplitter rozděluje paprsek ze zdroje na dva stejné paprsky. Jeden je odražen na pevné zrcadlo, od kterého se odrazí zpět. Druhý projde beamsplitterem a dopadne na pohyblivé zdrcadlo. Oba paprsky se odrazí a dopadnou zpět na beamsplitter, kde interferují a výsledný paprsek je znovu zčásti odražen k detektoru a zčásti projde beamsplitterem směrem ke zdroji. Intenzita výsledného paprsku je závislá na rozdílu vzdáleností obou zrcadel od beamsplitteru. Vlevo vzadu je elektronika, elektrický zdroj a vpravo je zdroj IR záření a laser, který měří vzdálenost pohyblivého zrcadla v interferometru.

Vpravo je použitý, ale stále funkční zdroj IR záření, vlevo je nový, nepoužitý. Tento zdroj se označuje jako Globar, což je lampa s tyčinkou z SiC. Dříve se používala Nerstova lampa, což je keramická (ZrO2 a Y2O3) tyčinka, která za vysoké teploty svítí v infračervené oblasti. Před měřením se Globar nahřeje na teplotu zhruba 1100 °C a při této teplotě vydává infračervené záření.
Podle optické soustavy rozlišujeme spektrometry:
- Disperzní
- Nedisperzní
- Interferometrický spektrometr
Disperzní - za vzorkem je umístěn monochromátor (mřížka), který postupně propouští jednotlivé vlnové délky na detektor. Nedisperzní využívá monochromatické zdroje záření. Interferometrický spektrometr neobsahuje monochromátor, ale Michelsonův interferometr. Celé spektrum snímá najednou a vzniká interferogram, který je nutné zpracovat pomocí Fourierovy transformace a je citlivější než ostatní typy spektrometrů.
Interpretace spekter
[editovat | editovat zdroj]Výšku absorbance každého vibračního pásu ovlivňuje koncentrace dané látky, molární absorpční koeficient. Tedy čím nižší koncentrace, tím nižší absorbance.
Pík neboli vrchol či maximum (v absolutní hodnotě, tudíž i minimum). Zde máme ukázku transmisního spektra toluenu.

Takto vypadá jeho strukturní vzorec.
První zvýrazněná oblast (zleva) je vazba C-H valenční, jedná se o vibraci C-H vazby vodíku ve skupině methylu. Druhá oblast je oblastí overtonů (přechod molekuly do excitovaného stavu) a kombinačních vibrací. Třetí oblast obsahuje píky vazby C=C v benzenovém kruhu. Čtvrtá obsahuje deformační vazby C-H v rovině benzenového jádra (atomy H kmitají k benzenu a od něj) a v páté oblasti jsou atomy H kmitající mimo rovinu benzenu.
Ze spektra lze vyčíst následující informace:
- Poloha pásů - je dána rozdílem energií hladin, mezi kterými systém přechází. Využívá se ke kvalitativní analýze, z polohy pásů lze určit, které vazbě daná vibrace odpovídá. Polohu pásů lze určit jako lokální maximum/minimum na křivce, podle typu měřené veličiny (absorbance vs. transmitance).
- Pološířka pásů (FWHM) - může nést informaci o kvantitě, příp. o některých pochodech, např. Berryho pseudorotaci
- Hodnota absorbance - využívá se ke kvantifikaci (Lambertův-Beerův zákon)
- Integrální intenzita - využívá se ke kvantitativní analýze. Integrací získáme obsah plochy pod křivkou ve dvourozměrné rovině. Integrální intenzita se používá ke stanovení relativní koncentrace látek v roztoku díky změření plochy pod píkem. Toto je často problematické vzhledem k~možnosti překrývání jednotlivých píků.
- Tvar pásu - lze také využít k analýze spektra.
Zde je tabulka nejcharakterističtějších skupin a jejich vlnočtů v IR spektroskopii:
| Sloučenina | Skupina | Vlnočet [cm-1] |
|---|---|---|
| Alkany | C-H | 2850-3000 |
| C-C | 800-1000 | |
| Aromáty | C–H | 3000-3100 |
| C–C | 1450-1600 | |
| Alkeny | C–H | C–H |
| C–C | 1630-1670 | |
| Alkyny | C–H | 3300-3320 |
| C≡C | 2100-2140 | |
| Alkoholy | O–H | 3300-3600 |
| C–O | 1050-1200 | |
| Aldehydy | C=O | 1720-1740 |
| C–H | 2700-2900 | |
| Karboxylové kyseliny | C=O | 1700-1725 |
| O–H | 2500-3300 | |
| C–O | 1100-1300 |
